Market Overview
複雑な課題が新たな機会を生む
日本の医療機器市場は大きな成長と利益の可能性を秘めています。日本は世界第3位の医療機器市場であり、 2024年から2028年の間に年平均成長率(CAGR) 6.75%で、総額155億6千万ドルの成長*
が見込まれています。テクノロジーの進んだ高齢化社会である日本は、医療イノベーションに対して非常に高い価値を置いています。
海外の医療機器メーカーや新興企業にとって、日本の薬事規制をクリアするのは複雑で困難の多いプロセスとなり得ます。日本における医療機器の承認や認証には厳格な要件が定められており、プロセスガイドラインの遵守が求められます。膨大な書類作成と厳格な品質管理対策が伴うため、成功するには知識豊富なパートナーの存在が極めて重要になります。経験豊富な選任製造販売業者(DMAH)の存在は、日本の医療機器規制を確実に遵守するために不可欠です。
日本の医療機器市場の洞察:2032年までの予測
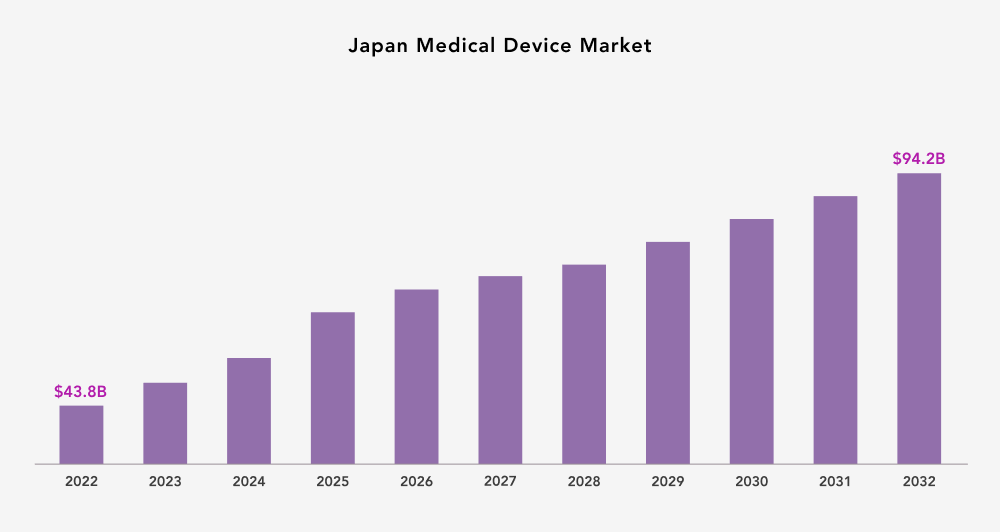
(Source: Spherical Insights)
- 2022年の日本医療機器市場規模の評価:438億6,000万ドル
- 2022年から2032年までの年平均成長率:7.95%
- 日本医療機器市場規模予測:2032年までに942億3,100万ドル突破。
日本の医療機器収益 2018〜2028年(セグメント別)
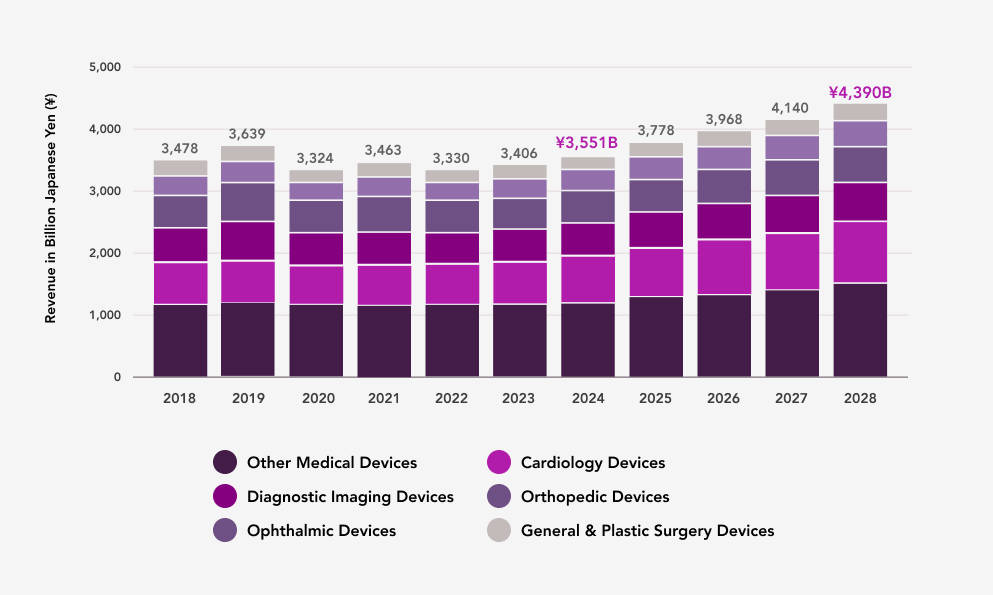
Source: Published by Statista Research Department, Feb 9, 2024
- すべての医療機器セグメントで大幅な増収を予測
- 市場最大のセグメントは心臓関連機器で、2024年の市場規模は52億ドルと予測
MCRAジャパンの業績

選任製造販売業者(DMAH)
特例承認制度により、日本の医療機器市場での主体性を高めることができます。
日本の薬事制度は、製造販売業許可を有する企業の薬事申請を前提としています。そのため、医療機器を日本に輸入して日本市場で販売することができるのは、製造販売業者(MAH)または選任製造販売業者(DMAH)の資格を有する日本国内の法人のみです。海外の医療機器・製薬企業が、日本で製品を販売するには、日本の行政機関に対応できる製造販売業者(MAH)や選任製造販売業者(DMAH)を選任し、薬事承認を取得する必要があります。

![]()
DMAHとは?
外国特例承認制度により外国の医療機器製造業者(海外メーカー)から選任されるDMAHは、海外メーカーの国内代理人に当たります。
海外メーカーはMCRAジャパンをDMAHとして選任することにより、MCRAジャパンの国内インフラと人材を活用できるため、日本法人を設立し、製造販売業許可を取得するなどの初期投資を最小限に抑えつつ、自社の参入戦略に関する業務全般のコントロールを維持することができます。
DMAHは、製品の薬事承認取得のサポートから承認後の海外メーカーの代理としての薬事業務を行います。
DMAHの主な業務:
- 薬事承認申請、外国製造業者登録など日本市場参入のための許可取得。
- 製品の輸入、保管、検査、流通の管理
- 変更管理による承認維持
- QMS省令に基づく品質管理
- GVP省令に基づく製造販売後安全管理
MCRAジャパンのDMAHサービスの利点
- クラスII以上の全リスクレベルの医療機器に対応
- 熟練した薬事および臨床のエキスパートスタッフが、後発、改良から新医療機器まですべての薬事申請に対応
- バイリンガルかつ多文化的背景を持つ優秀なサポートスタッフが、明確かつ効果的に薬事エキスパートや当局とのコミュニケーションをサポート
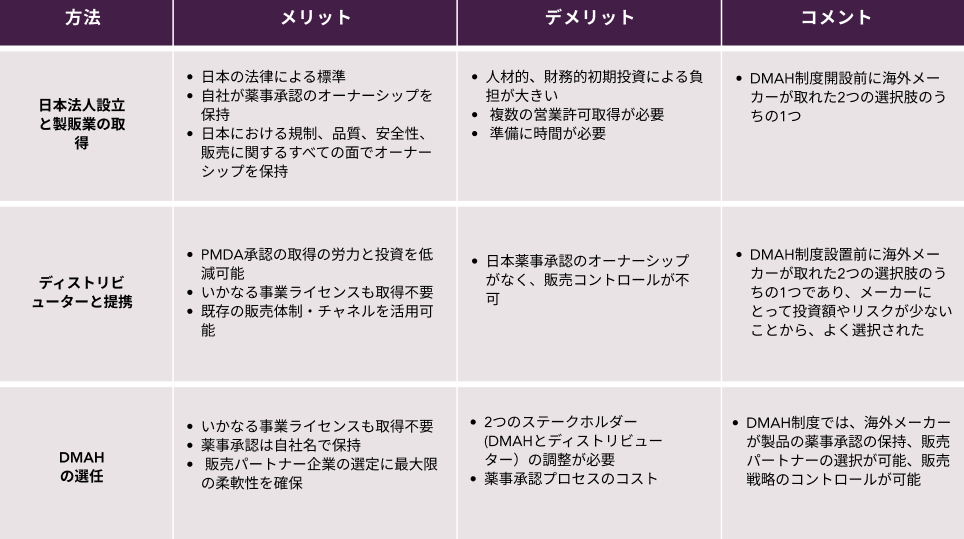
海外メーカーが日本で医療機器を事業化するには、3つの方法があります。